致命罕见病有望迎来首款基因疗法 已启动临床试验
日前,基因疗法公司Myonexus Therapeutics宣布启动一项评估新型基因疗法MYO-101的临床试验,用于治疗β-肌聚糖病(LGMD2E)。该公司致力于与美国国家儿童医院(Nationwide Children’s Hospital)的基因疗法中心以及Sarepta Therapeutics合作,为肢带型肌营养不良症(LGMD)开发首个矫正基因疗法。他们的目标是向骨骼肌和心肌中递送一种基因,使β-肌聚糖(β-sarcoglycan)实现有力的功能性表达,该蛋白质的缺乏会导致LGMD2E。该试验中第1队列的首位患者于10月开始接受治疗,估计其余患者将在今年内完成治疗。
LGMD2E是由基因突变引起的罕见、退行性且通常致命的肌营养不良症。这些患者的进行性肌纤维损失、炎症和瘢痕,会导致肌肉力量和功能的退化。该疾病导致过早死亡的主要原因之一,是由心脏组织损伤引起的心肌病。这些患者急需有效疗法来缓解疾病,延长生命。
Myonexus的基因疗法平台使用AAVrh.74载体系统,该平台在获得许可之前,已由来自美国全国儿童医院的研究团队评估超过12年。MYO-101的临床前研究表明,载体能够被稳定转导至骨骼肌和心肌,并且没有治疗限制性免疫应答。在小鼠模型接受过一次MYO-101治疗后,其超过95%的肌肉细胞能产生β-肌聚糖蛋白,并且功能性关键参数(包括强度和心输出量)也趋于标准水平。与未经治疗的小鼠相比,该治疗与肌纤维直径增加、瘢痕和脂肪浸润减少以及总体活性改善相关。
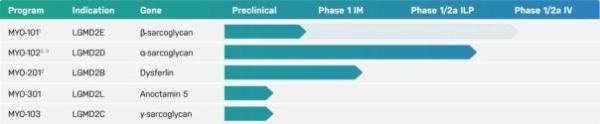
▲Myonexus研发管线(图片来源:Myonexus Therapeutics官网)
Myonexus总裁兼首席执行官Michael Triplett博士说:“通过使用高度精确的载体技术,基因疗法具有巨大潜力,为挑战性罕见病提供功能性治疗解决方案。基于临床前研究在有效性和安全性方面的积极结果,我们对MYO-101的载体和平台充满信心,并希望MYO-101能成为首个用于LGMD2E患者的深度疗法。我们期待与LGMD群体合作,并相信通过倾听和整合他们的反馈,将共同给这种疾病的进展带来巨大影响。”
Myonexus首席科学官兼Sarepta Therapeutics基因疗法副总裁Louise Rodino-Klapac博士说:“在MYO-101中使用的载体已经被评估超过十年,在临床前研究中,我们看到该载体能有力一致地转导至骨骼肌和心肌中,并能显著恢复缺失蛋白水平。如果临床试验能取得成功,这有望成为LGMD2E的首个矫正疗法,这是一种无情的疾病,会掠夺患者的力量和生命。”
美国国家儿童医院Curran-Peters研究主席Jerry Mendell博士说:“MYO-101是多年努力和实验的结晶。它与我们用于杜氏肌营养不良症的微抗肌萎缩蛋白(microdystrophin)基因疗法项目有很多共同之处,它也针对骨骼肌和心肌,恢复肌营养不良蛋白相关蛋白复合物中的一种重要缺失蛋白,并与微抗肌萎缩蛋白构建体共享一个相同的病毒衣壳和启动子。我们期待随着首批LGMD2E试验参与者开始治疗,我们能继续推动这项基因疗法的开发。”
参考资料:
[1] Myonexus Therapeutics Announces the Initiation of a Trial for the First-Ever Gene Therapy for Beta-sarcoglycanopathy, Also Known as Limb-Girdle Muscular Dystrophy Type 2E. Retrieved Nov 9, 2018, from https://www.biospace.com/article/releases/myonexus-therapeutics-announces-the-initiation-of-a-trial-for-the-first-ever-gene-therapy-for-beta-sarcoglycanopathy-also-known-as-limb-girdle-muscular-dystrophy-type-2e/?keywords=beta+sarcoglycanopathy
[2] Myonexus Therapeutics. Retrieved Nov 9, 2018, from http://myonexustx.com/
来源:新浪医药
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}