药明康德2023年十大科学突破榜单正式发布。在这份榜单中,有让我们全面认识人类自身的重磅进展;有探寻生命起点的技术革新;也有已经获批上市,正在改写治疗格局的创新疗法。它们构成了今年生物医学领域最受瞩目的瞬间。接下来,让我们共同揭晓这份定义了2023的年度榜单。
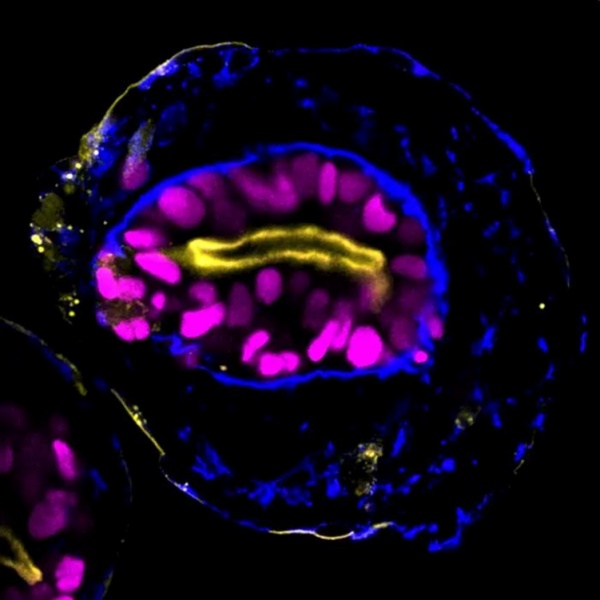
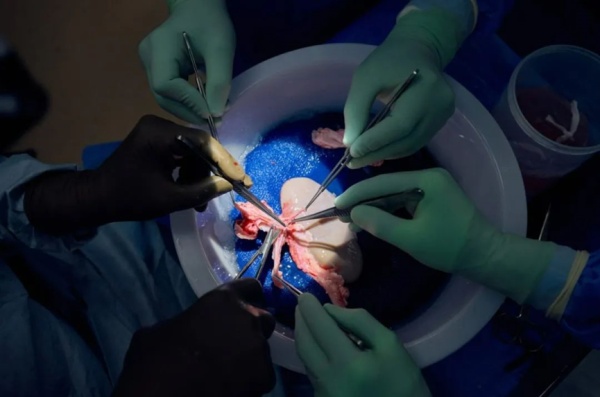
▲《科学》杂志封面介绍了脑细胞普查项目(图片来源:Ivana Kapustová and Sten Linnarsson,瑞典卡罗林斯卡医学院和艾伦脑科学研究所/ Science官网)今年10月,《科学》杂志发布了“脑细胞普查”(Brain Cell Census)专题,一共21篇研究论文同步在《科学》及其子刊上线,这些成果汇集了全世界数百名来自来“脑计划-细胞普查网络”项目的科学家的共同努力。该项目的众多科研小组利用先进的单细胞测序等技术开展了一系列研究,尤其是从单细胞层面以前所未有的颗粒度解析了人脑的组织结构,包括成年人脑和胚胎期正在发育的人脑。这些论文共同识别和描绘出了人脑细胞类型的惊人多样性,为认识人类精神和神经疾病的机制提供了线索,也让我们对人类这一物种的身份有新的认识。从此,对人脑的研究进入“细胞时代”。▲来自其中一项研究的人工胚胎模型展现出类似于植入后人类胚胎外胚层的结构(图片来源:剑桥大学)长期以来,人类胚胎最初两三周的发育过程处于难以理解的“黑匣子”状态。2023年,来自英国、美国、中国、以色列的多个研究团队在“人工创造人类胚胎模型”上的突破性进展,揭开了这段“黑暗时期”的秘密。采用不同的策略方法,科学家们实现了在无需精子和卵子的情况下,完全利用人类干细胞,在体外制造出与人类胚胎十分类似的组织结构。这类“人工合成胚胎”可模拟人类胚胎最初两三周的发育过程与关键特征,为阐明早期人类发育带来前所未有的机会,有助于更好地理解出生缺陷的致病机理并找到避免缺陷的策略。▲GLP-1激动剂当选《科学》期刊的2023年度科学突破(绘图:Stephan Schmitz;图片来源:Science官网)在生物医药领域,胰高血糖素样肽-1(GLP-1)无疑是今年的热词。GLP-1激动剂早已获批用于2型糖尿病的治疗,而近年来,GLP-1相关药物与肥胖症的关系开始受到关注。以司美格鲁肽、Zepbound为代表的GLP-1药物相继获美国FDA批准用于肥胖症治疗;一款名为retatrutide的三靶点药物更是在今年的临床试验中取得11个月平均减重24.2%的成绩。这些创新性减肥疗法有望带来更多的治疗选择和更好的治疗效果。与此同时,大量研究正在探索GLP-1药物的其他健康收益或是威胁,这提醒我们:对于这类药物,我们还需要更全面、深入的认识。▲利用细胞“性转”策略产下的小鼠(图片来源:DOI: 10.1038/s41586-023-05834-x)在自然界,哺乳动物的繁殖无疑需要雌雄两种性别个体的结合。但现在,科学家们正在让“同性繁殖”成为可能。在今年的一篇《自然》论文中,研究团队利用干细胞和染色体工程技术设计了一种细胞“性转”策略,引导雄性小鼠的干细胞转换性别并形成可受精的卵细胞。部分卵细胞成功受精,最终诞生出健康可育的后代。同期的评论文章指出,这项进展标志着生殖生物学的一个里程碑,领导这项研究的日本科学家林克彦教授也入围了《自然》年度十大人物。在该技术最终在人类中可行之前,相信围绕着生物伦理的讨论也必不可少。▲CAR-T细胞疗法(图片来源:药明康德内容团队)CAR-T细胞疗法已经成为治疗血液癌症的革命性疗法,现在,这类疗法又向自身免疫病发起了挑战。抗合成酶抗体综合征(ASS)是一类严重的肌炎,这种由免疫系统故障引发的疾病可激发肺间质病变,因此病情进展迅速、死亡率高。在《柳叶刀》杂志的论文中,埃尔朗根-纽伦堡大学团队利用CAR-T细胞疗法成功治愈一名ASS患者。停用免疫抑制药后,患者的症状依然在持续好转。这也是该团队在治愈系统性红斑狼疮后,利用CAR-T细胞疗法治愈的第二种自身免疫病。▲《自然》封面专题介绍了首个人类泛基因组参考草图(图片来源:Darryl Leja/NHGR;Nature官网)2023年,人类遗传学研究迎来一个新的里程碑:首个人类泛基因组参考(human pangenome reference)草图发布。2022年,首个完整的人类参考基因组已经发布,但原有的单一参考基因组大部分序列来自一个志愿者,因此存在局限性。现在,来自《自然》专题的最新图谱结合了来自不同祖源的47个个体的遗传信息,能更全面、更准确地反映全世界人类的遗传多样性。新的泛基因组参考图谱还比原有的参考基因组序列多了1.19亿个新碱基,尤其丰富了对结构变异的识别,因而可以更准确地发现和评估与疾病有关的遗传变异。▲CRISPR基因编辑(图片来源:药明康德内容团队)11月17日,全球见证了生物技术的一个全新里程碑。一款基于CRISPR基因编辑技术的疾病疗法,获得了英国药品和健康产品管理局(MHRA)的有条件上市许可,成为全世界首款获得监管机构批准上市的CRISPR基因编辑疗法。这款商品名为Casgevy的疗法获批用于治疗输血依赖型β-地中海贫血以及镰刀状细胞贫血病这两种遗传性血液疾病。在长期随访中,接受治疗的患者相关疾病症状消失,并且不再接受输血需求,基因编辑治疗让他们重获新生。12月9日,美国FDA也批准Casgevy疗法上市用于治疗镰刀型细胞贫血病,其也成为FDA批准的首款CRISPR基因编辑疗法。这把“基因剪刀”已经成为人类对抗疾病的有力武器。▲研究团队正在去除猪肾脏多余的组织,准备用于人体移植(图片来源:Joe Carrotta for NYU Langone Health)近年来,猪器官异种移植成为了解决供体器官短缺的潜在方法。去年,全球首例猪心脏人体移植手术成功完成;2023年,猪肾脏移植领域迎来了全新的里程碑。阿拉巴马大学团队成功地将经过基因编辑的猪肾脏移植到人体后,肾脏可以持续运作一周,并且提供机体运转所需肾功能。纽约大学团队也同时发布了阶段性进展:将基因编辑的猪肾脏移植到一位脑死亡者体内后,肾脏存活并发挥功能长达32天,这也是猪肾脏首次在人体正常工作超过一个月。值得一提的是,在近期的《自然》论文中,接受人源化猪肾的食蟹猴在移植后存活了超过2年,验证了长期存活的潜力。▲借助这套装置,患者可以在拐杖的帮助下自然行走(图片来源:洛桑大学附属医院/Gilles Weber)当大脑与控制行走的脊髓区域之间的通信受损,很多患者终生只能与轮椅相伴。现在,新技术的涌现让事情有了转机。瑞士洛桑联邦理工学院(EPFL)的科学家开发了一种脑-脊髓接口(BSI),通过解析大脑发出的信号并刺激参与行走的脊髓区域,帮助因脊髓损伤而四肢瘫痪的患者恢复运动能力。一名已经瘫痪12年的患者在植入该设备后,成功地通过自己的意识夺回了对双腿主要关节的控制权。经过康复训练,这名患者已经重新能够自然站立和行走,甚至爬楼梯、跨越障碍。研究还发现,该装置还能促进神经恢复。正如这名患者所言:“以前是电刺激控制我,现在我可以用思想控制它。”▲《细胞》封面展示了记忆储存的过程(绘图:Julia Kuhl;来源:Cell官网)我们知道,短期记忆形成于海马体,而稳定的长期记忆则是储存在大脑皮层中。但记忆从海马体向大脑皮层转移的中间过程,却是个长期未解的难题。现在,洛克菲勒大学的科学家团队开发出一项全新的单细胞分辨率多区域成像技术,能够连续数周观测海马体与皮层中间区域神经元,实现了对该区域神经元活动的连续追踪。由此,这项研究首次解析出长期记忆转移的中间过程,发现此前往往被忽略的前端丘脑是处理、巩固记忆的关键中转站。








{replyUser1} 回复 {replyUser2}:{content}