近20年的执着,礼来阿尔茨海默病疗法能否顺利越过上市终点线?
阿尔茨海默病(AD)是老年人中最常见的神经退行性疾病,对患者本身、他们的家庭,乃至社区和整个社会都有相当严重和深远的负面影响。然而,开发治疗AD的有效疗法一直以来都是一个艰巨的挑战。
不过,随着产业与学术界的共同努力,AD领域在近年迎来着激动人心的突破。2023年7月,靶向淀粉样蛋白(Aβ)的抗体疗法lecanemab(商品名:Leqembi)获得了FDA的完全批准,成为了20年来FDA首次完全批准的AD疗法。而最有希望成为第二款获得美国FDA完全批准,靶向Aβ的AD疗法的,可能要数礼来(Eli Lilly and Company)的donanemab了,该候选疗法目前正在接受美国FDA审评,预计近期就会公布最终结果。
自步入临床试验以来,donanemab的表现一直都很出色。不过,很少有人知道,donanemab的研发过程也几经波折,但礼来的研发团队每次都坚定地选择继续前行,才使得这款具有巨大潜力的疗法走到了现在。在今天的这篇文章中,药明康德内容团队将结合公开资料,为大家道来donanemab背后的故事。

前途未卜的溶斑抗体
21世纪初,由于强有力的遗传和生化证据强调了淀粉样蛋白通路在AD发病机制中的核心作用,“淀粉样蛋白假说”开始兴起,随后引发了Aβ靶向AD疗法的开发浪潮。Donanemab的起源也可以追溯到这一时期,礼来的罗纳德·德马托斯(Ronald DeMattos)博士在这款疗法的研发过程中起了重要作用。
那时,整个AD疗法开发领域尚处于一片混沌之中。尽管针对“淀粉样蛋白假说”衍生出了多种治疗策略,例如预防自由淀粉样蛋白的形成、去除现有淀粉样蛋白或分解大脑中的淀粉样蛋白斑块等,但没人知道它们究竟会不会奏效。这种情况令当时礼来公司中很多内部人士都对是否要继续在淀粉样蛋白靶向疗法的开发中增加投入而摇摆不定。
图片来源:123RF
但德马托斯博士并未受到干扰。基于他多年来在AD治疗领域积累下来的经验,他多次明确地向礼来的管理层指出,没有数据表明淀粉样蛋白这个靶点存在问题。不过,要开发出一款能够直接破坏大脑中淀粉样蛋白斑块的抗体疗法,德马托斯博士面临的挑战也很多。
首先是,针对淀粉样蛋白斑块的抗体会不会被人体的免疫系统拦截?是否能顺利进入大脑?其次,如何能开发出不会与淀粉样蛋白单体结合,只与淀粉样蛋白斑块产生相互作用的抗体?第三,当时大多数抗体疗法的设计目标都只是用来预防淀粉样蛋白斑块的形成,但德马托斯博士认为这与临床中的实际需求并不相符——临床中的AD患者均已形成了淀粉样蛋白斑块,他们最需要的应该是能够去除淀粉样蛋白斑块的疗法。这就要求使用到的淀粉样蛋白动物模型足够可靠,其临床前机制验证结果才可信。
不过,兵来将挡,水来土掩。德马托斯博士最终还是一步一个脚印地解决了这些难题。
披荆斩棘入临床,首批数据险折戟
对于该如何设计候选抗体这个问题,德马托斯博士认为,如果候选抗体进入血液后就直接与血液中的自由淀粉样蛋白单体发生结合,那就根本没有机会进入大脑发挥作用了。因此,他想设计一种只与大脑中的淀粉样蛋白斑块结合的抗体,这种抗体能够跳过淀粉样蛋白单体和寡聚体的“障碍”,更有效地清除大脑中的淀粉样斑块沉积。
功夫不负有心人,德马托斯博士在对大脑中的淀粉样斑块进行细致研究后发现了一种特定的环状结构,该结构被命名为N3pG。在与两位抗体科学家日夜兼程的共同努力下,靶向N3pG淀粉样蛋白亚型的抗体donanemab诞生了。Donanemab旨在特异性地与大脑中的淀粉样斑块相结合,从而促进淀粉样斑块的清除。
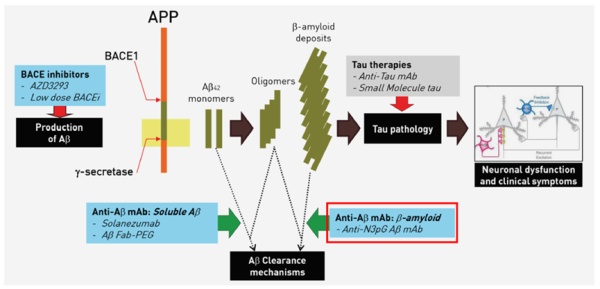
▲Donanemab旨在特异性地与大脑中的淀粉样蛋白斑块相结合,从而促进它们的清除(红框标注的位置,图片来源:参考资料[4])
为了获取可靠的临床前研究数据,顺利将donanemab推入临床,德马托斯博士没有选择礼来公司现有的淀粉样蛋白小鼠模型——这些模型小鼠距离初代小鼠接受基因改造已有十余年,其基因组已发生漂移,因此不同的小鼠可能展现出不同的疾病特征,这将影响试验结果的一致性。
严谨的德马托斯博士花费了4年的时间,终于培育出了一批小鼠模型,这些小鼠脑中的淀粉样斑块水平与AD患者的相似。他的努力最终没有白费,在临床前实验中,donanemab成功使小鼠大脑中的淀粉样斑块水平急剧下降!
这一喜人的结果让donanemab于2011年进入了临床研究,但接踵而至的却是一个差点让该疗法终止开发的坏消息。在这项1期研究中,研究人员最先获得的数据显示,超过90%的患者都对donanemab产生了抗药抗体。这不得不令人怀疑,donanemab是否能够进入大脑,因为它们很可能在到达大脑前就被抗药抗体消耗完了。如果事实真是如此,那这项临床试验也没有继续开展的必要了。
难道donanemab就要这样夭折了吗?
还好,礼来公司此前的一个决定将donanemab从“死亡线”上拯救了回来。2010年时,礼来收购了Avid Radiopharmaceuticals公司,并获得了该公司正在开发的一种可用于检测大脑中淀粉样斑块的分子显像剂florbetapir。这种显像剂可以粘附在淀粉样蛋白上且具有放射性,研究人员通过正电子发射断层扫描(PET)技术扫描患者大脑看到florbetapir亮起的部位就意味着淀粉样蛋白的存在。此前,确认AD患者大脑中淀粉样斑块的存在只能通过解剖来实现,而在这种成像技术的帮助下,研究人员能够直接观察到AD疗法对患者大脑中淀粉样蛋白斑块的作用。
Florbetapir的存在为donanemab争取到了一个机会,研究人员决定再观察一段时间,看看donanemab是否真的一点希望都没有了。
随后获得的脑扫描结果令所有人都感到震惊。尽管患者对donanemab产生了免疫反应,但它仍能使患者大脑中的淀粉样蛋白持续且迅速地减少,甚至在那些只接受过1次给药的患者中也是如此!不仅如此,接受donanemab多次给药的许多患者中,其脑部的淀粉样蛋白竟然完全清除了!
这项研究的结果令所有人都意识到了donanemab所具有的潜力,礼来公司随后开始全力以赴地推动donanemab的上市进程,首先是从启动2期临床试验开始。
临床试验设计精细,疗效数据令人惊艳
我们知道,除了药物的特性,临床试验的设计和实施方式的差异也会对确定药物的临床效果产生重大影响。对于AD疗法开发来说,在临床试验中选择合适的受试者是重中之重。在疾病早期刚出现淀粉样蛋白沉积时就使用清除沉积的疗法可能会有一定的效果,但在大脑已经出现神经炎症之后,单纯清除淀粉样蛋白沉积的效果就不会太好了,因为这时候神经炎症造成的大脑神经细胞的死亡,可能比淀粉样蛋白沉积更为严重。
Donanemab的2期临床试验总计入组了272名早期AD患者。研究人员在筛选患者时不但检测了他们的认知能力,还通过成像手段对其大脑的淀粉样蛋白和tau蛋白的沉积进行了检测。Tau蛋白与淀粉样蛋白沉积一样,是AD患者大脑中的标志性特征,它的出现一般比淀粉样蛋白沉积要晚,与患者认知水平下降的相关性更为密切。这种筛选方法确保了纳入的患者符合试验要求,这些患者的病情不会过于轻微,也不会过于严重以至于无法从治疗中受益。

图片来源:123RF
2021年1月,礼来公司宣布这项2期临床试验达到了主要临床终点,donanemab将评估早期阿尔茨海默病患者认知能力和日常功能的综合指标的下降速度延缓了32%。此外,对淀粉样蛋白沉积的成像检测显示,接受donanemab治疗的患者大脑中的淀粉样斑块大幅度减少。基于这项研究的积极结果,同年6月,donanemab获得了美国FDA授予的突破性疗法认定。
2023年7月,礼来再次交出了一份更令人满意的3期试验的完整答卷。在3期临床试验TRAILBLAZER-ALZ 2中,donanemab可显著减缓具有AD早期症状患者的认知与功能下降、延缓疾病进展。亚群分析显示,处于疾病最早阶段的受试者获益更为显著,与安慰剂相比,其认知与功能下降减缓达60%。此外,无论患者基线时的病理分期为何,donanemab治疗都能显著降低其淀粉样斑块水平。在18个月时,在所有受试者中,donanemab治疗使淀粉样斑块平均减少84%,而此数值在安慰剂组患者中仅为1%。
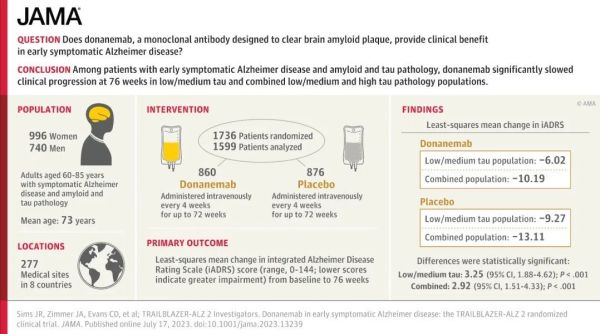
▲TRAILBLAZER-ALZ 2试验设计与结果摘要(图片来源:参考资料[5])
在该临床试验中还有一项创举是,当患者达到预定的淀粉样斑块清除的标准时,受试者就能够停止使用donanemab。这意味着,AD患者们在治疗中有了一个明确的停药标准,有望使患者减少不必要的治疗。该研究中,约一半的受试者在12个月时达到停药标准,而约每10名受试者中有7名在18个月时可达到此标准。
2023年第二季度,礼来已向美国FDA递交了上市申请,我们也将在近期迎来这款疗法的最终监管审批结果。期待礼来近20年的执着能够获得成功,为广大AD患者带来新的治疗选择。
来源:药明康德
版权及免责声明:本网站所有文章除标明原创外,均来自网络。登载本文的目的为传播行业信息,内容仅供参考,如有侵权请联系答魔删除。文章版权归原作者及原出处所有。本网拥有对此声明的最终解释权。


{replyUser1} 回复 {replyUser2}:{content}